فاولينج القشور
وصف الظاهرة:
تحدثنا من قبل عن طبيعة مياه التغذية فى بدايات الجزء الأول من كورس التناضح العكسي …
وذكرنا موضوع القشور أو الscales وترسب الأملاح على الأغشية وقلنا أن أهم الأملاح التى تسبب تكون القشور هى أملاح العسر(كأملاح الكالسيوم والمغنسيوم)
… ونضيف هنا أن هذه القشورعادةً ما تترسب فى المراحل الأخيرة من الأغشية وهو ما نسميه أغشية الذيل (Tail membranes) لأنها نهاية محطة الأغشية والسبب فى ذلك هو القابلية للترسيب فى تلك المرحلة نظراً لزيادة التشبع وزيادة تركز الأملاح بالمقارنة بالأغشية الأولى …
ففى المراحل الأولى من الأغشية تمر مياه قد تم معالجتها من الأملاح المسببة للقشور وبالأخص أملاح الكالسيوم والمغنسيوم … حيث تم التخلص من النسبة الأكبر منها أو إضافة كيماويات مثل الأحماض أم مضادات القشور (الأنتى سكيل) تمنع ترسبها على الأغشية … تم ذلك فى المعالجة الإبتدائية … وتم خفض الLSI إلى الصفر أو الأقل من الصفر …
مما يساعدنا فى انتاج حجم أكبر من المياه (الريكافرى) بدون الخوف من ترسب الأملاح.
نعم …
أصبح امكانية ترسب الأملاح منعدمة فى البداية … شىء جميل جداً …
ولكن مع التقدم فى مراحل التحلية بالأغشية … والمياه الريجيكت التى خرجت من الأغشية الأولى فى وعاء الضغط الأول تحمل أملاحاً بتركيز أعلى من مياه التغذية التى دخلت على الأغشية فى البداية … ستصبح هى نفسها مياه التغذية للأغشية التالية وأوعية الضغط التالية وهكذا يزيد تركيز الأملاح من غشاء لغشاء ويصل ذروته فى نهايات الأغشية (أغشية الذيل) ونصل إلى درجة التشبع Saturation (ويزيد الLSI)مرة أخرى …
كما أن الcross flow الذى يسبب كسح “أو كنس” Sweeping للأملاح فى هذه الأغشية يكون أقل ما يمكن بالمقارنة بالأغشية القائدة كما ذكرنا من قبل …
لذا فإن الأملاح تجد البيئة الهادئة للاستقرار والاسترخاء على سطح الغشاء.
تبدأ أول مراحل الترسبات حيث تتشكل بلورات (كريستالات) الأملاح تشكيلاً مبدأياً فى مرحلة نسميها pre-clustring أو مرحلة ما قبل تكون عناقيد البلورات … وهذه البلورات تكون مصيدة لجزيئات أخرى من الأملاح فوق مرحلة التشبع …
تتراكم بعضها فوق بعض لتكون بلورات ضخمة تترسب على سطح الأغشية وتسبب المأساة …
وفى الحقيقة … فإن ديناميكية عملية الترسب مازالت غامضة وغير مفهومة بالكلية … ويؤثر فيها عدة عوامل مثل الحرارة والpH والتركيب الكيميائى للأملاح نفسها والزمن اللازم لتكون بلورات هذه الأملاح المختلفة والتى نسميها فى العام الinduction time.
من صور الترسبات الكيميائية التى تظهر فى الأغشية: السيليكا …
والكاتيونات الموجبة: الكالسيوم والمغنيسيوم والباريوم والاسترانشيوم …
والكاتيونات السالبة: الكربونات والكبريتات والفوسفات …
وتسبب تكون القشورScales أعراض مهمة أهمها
ثقل وزن الغشاء وانخفاض فى تدفق البريميت نظراً لحدوث ترسبات تسد ثقوب الأغشية …
وهذه صورة تم عرضها من قبل تبين أكثر الأملاح تكويناً للقشور وأكثرها خطورة (من اليسار إلى اليمين):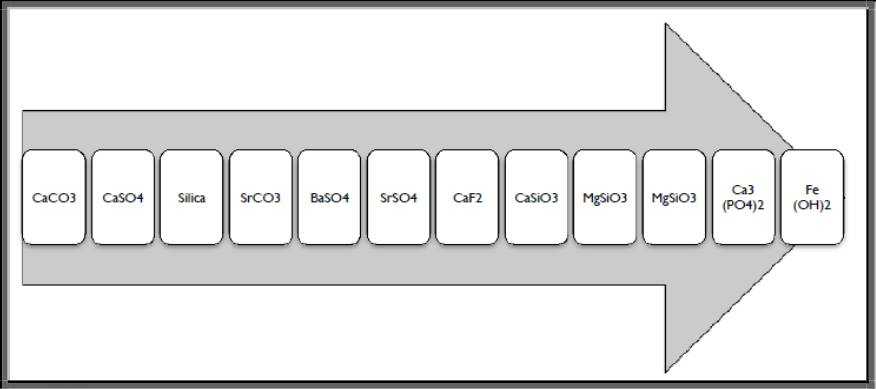
وإليك صورة مكبرة من البلورات الخاصة بقشور الكالسيوم والمغنيسيوم المترسبة على أغشية التناضح العكسي وهى تتشكل على هيئة طبقة رفيعة تسد مسام الأغشية وتقلل من كفائتها.
وهذه صورة مكبرة من ترسبات كربونات الكالسيوم CaCO3 على الأغشية تبدو كقطع صخرية تتناثر على أرض الصحراء:
وهذه صورة للأغشية وقد ترسبت عليها القشور الكلسية البيضاء:

وإذا حضرتك أضفت نقاط من حمض الهيدروكلوريك عليها فما يحدث هو فوران effervescence نتيجة تصاعد غاز ثانى أوكسيد الكربون … وهذا ما يُميز أملاح الكربونات عن الأملاح الأخرى (كأملاح الكبريتات Sulphate):
CaCO3 + 2 HCl —> CaCl2 + H2O + CO2
وهذه صورة لغشاء قد أصيب بقشور كبريتات الكالسيوم:
(من محاضرة المهندس محمد موسي: مشكلة تكون قشور كبريتات الكالسيوم مشكلة كبيرة حيث أن إزالتها بالغسيل الكيميائى لا يُعطى النتيجة التى نبغيها … وإذا وصلنا للنتيجة المرجوة فإنه يحدث تهتك فى الأغشية لأن بلورات هذه الأملاح تكون على هيئة إبرية قوية ولها حواف حادة تسبب جروح فى الغشاء … ويظهر ذلك بعد الغسيل الكيميائى فيجد العاملون أن الأملاح أصبحت عالية فى البيرميت بعد حدوث تلف فى الأغشية … عند الضغط عليها بيديك قد تصيبك بجرح … وهذا هو الفرق بين كبريتات الكالسيوم وكربونات الكالسيوم حيث أن الأخيرة لها ملمس جيرى …) … وهذا إلى جانب اختبار حمض الهيدروكلوريك.
نظر الفرق بين بلورات كبريتات الكالسيوم الإبرية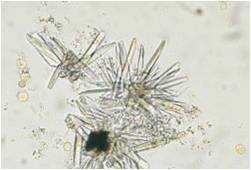
وكربونات الكالسيوم الحبيبية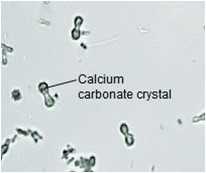
والحل التقليدي لكبريتات الكالسيوم هو إضافة أنتى ىسكيل مناسب له.
الكبريت العنصرى الأصفر هو أيضاً قد يترسب على الأغشية وربما على الBrine seal كما فى الصورة التالية نتيجة لأكسدة السلفايد بالأوكسجين أو الكلور أو أحد المعادن (ولذلك يجب أن لا يتعدى كبريتيد الهيدروجين فى مياه التغذية عن 0.1 جزء فى المليون حد أقصى).
2HS- + O2 —> 2So + 2OH-
وهذه صورة للأغشية وقد تراكمت عليها ترسبات رمادية بنية مشوبة باللون الأصفر من الكبريت العنصرى … والذى يسبب انخفاض فى الFlux وارتفاع فى الأملاح salt passage فى البيرميت:
أما قشور السيليكا فلنا فيها قصص وحوارات:
عنصر السيليكون Si يتواجد فى مياه أرضنا على هيئة ذائبة أو غير ذائبة …
إذا كان فى الصورة الذائبة فإنه يكون على هيئة سيليكا (SiO2) … سيلكون مرتبط بذرتين أوكسجين … وتتراوح نسبتها فى مياه التغذية ما بين 1 – 100 جزء فى المليون (وفى مياه البحر تكون ما بين 0.4 – 8 جزء فى المليون).
الشكل الكيميائى للسيليكا يتحدد تبعاً للpH.
الشكل السائد للسيليكا عند pH 7 أو أقل هو حمض الميتا سيليسيك Meta Silicic acid ورمزه الكيميائى (H2SiO3)n وهو حمض ضعيف يكون على هيئة من هذه الهيئات:
SiO2 – H2SiO3 – H4SiO4 (=Si(OH)4)
نلاحظ أن الn تشير إلى عدد الجزيئات.
فإذا حدث التشبع لهذا الحمض فى الماء وتعداه يعنى حدث Supersaturation يعني فوق التشبع فإنه يكون بوليمر وتزيد قيمة الn لتتكون سلسلة طويلة من السيليكا الغروية الغير ذائبة Insoluble Colloidal silica أو تتكون سيليكا جل غير متبلورة أو غير منتظمة Amorphous silica gel … وهذه المركبات تسبب القشورعلى الأغشية.
فإذا حدث وأن زادت الpH عن نقطة التعادل وهى 7 فإن تركيز أيونات الهيدروجين يقل ويتفكك حمض ال Silicicإلى أنيون السيليكاتAnion silicate ورمزه (HSiO3-)n وهذا الأستاذ أيضاً لن يتركنا فى حالنا فهو يتحد مع الكاتيونات الموجبة مثل الكالسيوم والمغنيسيوم والحديد والمنجنيز والألمونيوم ليكون أملاح السيليكات الغير ذائبةInsoluble silicate مما يسبب أيضاً تكوين القشور.
ويظهر فاولينج السيليكا فى الاغشية الأمامية فى المعتاد … وللأسف بلورات السيليكا تسبب تشوه للأغشية ولا يُفلح معها الغسيل الكيميائى فى المعتاد.
أكدت الأبحاث على أن الألومنيوم والحديد المتواجدان فى مياه التغذية يترسب مع السيليكا حتى ولو كانت تحت التشبع Under saturation … ولذلك يجب أن يكون الحديد والألومنيوم أقل من 0.05 جزء فى المليون فى مياه التغذية حتى ولو كانت السيليكا أقل من درجة التشبع … وكما نرى عامل الpH أيضاً هام … كل ذلك يُراعى عند التحليل الكيميائى للمياه الخام … وبالأخص عند استخدام المروقات أو الكوأجيولانت التى تتكون من حديد أو ألمونيوم.
من تتبع الpH فى وحدة التناضح نجدها تقل من 7.5 مثلاً إلى 7 أو 6.5 أو أقل وهنا تكمن الخطورة بناءً على ما قلناه من تكون السيليكا الغروية أو الغير متبلرة مع زيادة التركيز وتتكون الترسبات.

ونجد فى الرسم البيانى التالى أن السيليكا تكون أكثر ذوبانية عند pH مرتفعة بعد الثمانية (ولكنها نشطة فى التفاعل مع الكاتيونات الموجبة كما قلنا وتقل ذوبانيتها حتى تنعدم ما بين 8.2 – 7 ثم ترتفع قليلاً عند pH أقل:
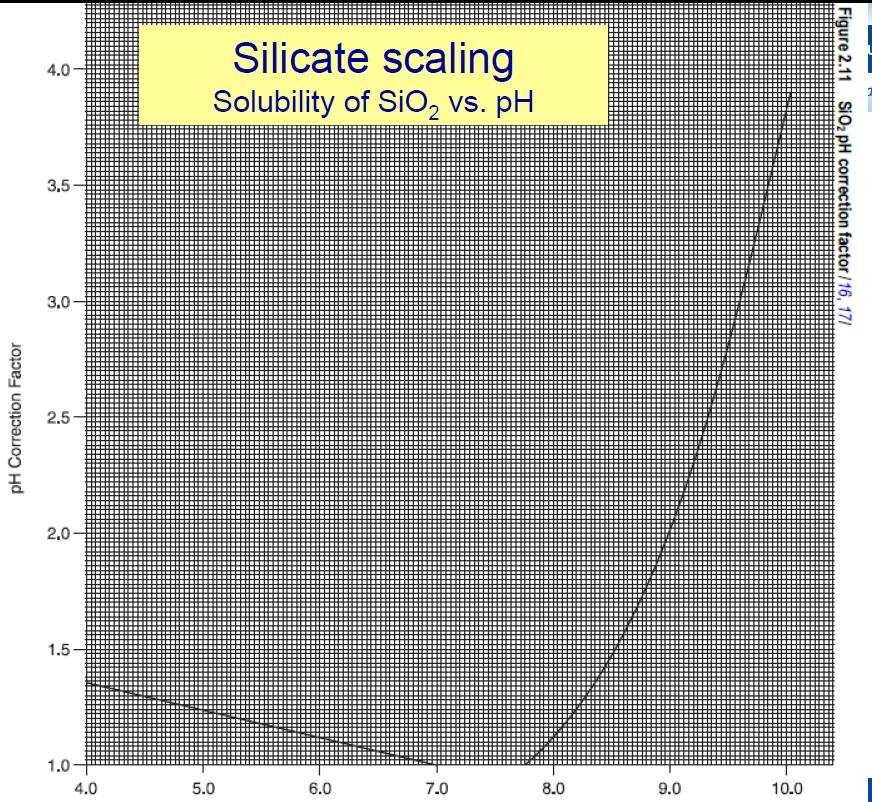
يضاً ذوبانية السيليكا تعتمد على درجة الحرارة (تناسب طردى) … انظر الرسم البيانى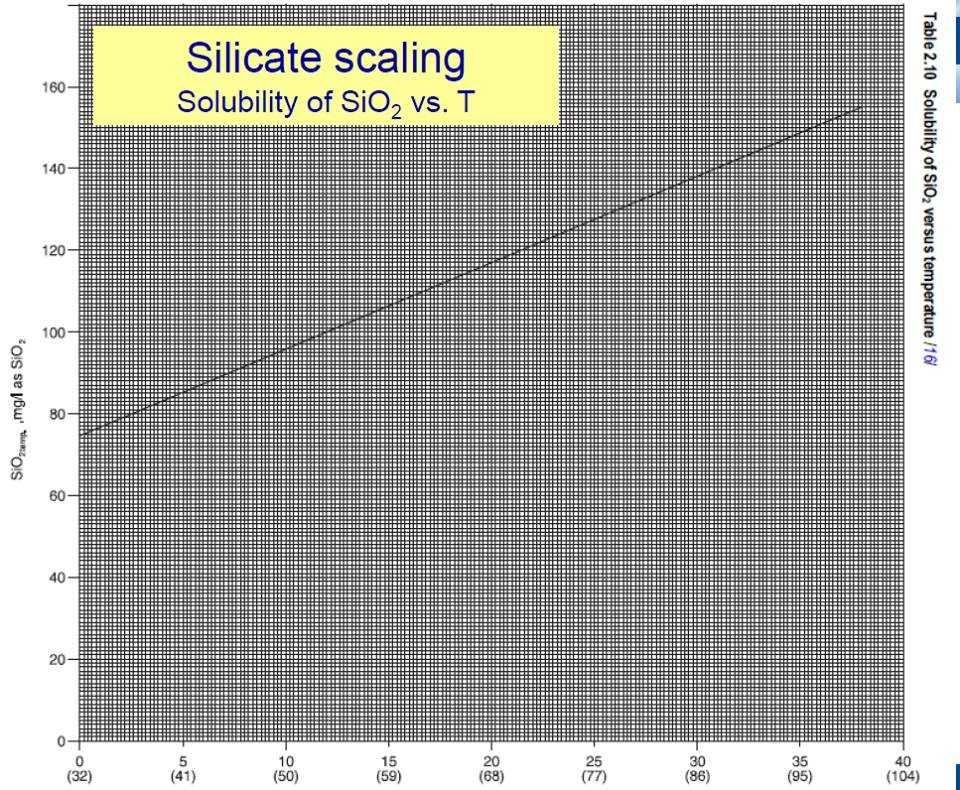
كى تتحاشى وتتفادى تكون قشور السيليكا فهو أمرهام سنترك لكم المجال لابداء الحلول المقترحة … خاصة عندما يكون تركيز السيليكا عالى فى مياه التغذية … هل الأفضل وضع مبادل أنيونى Anionic exchange resin قبل الدخول على الأغشية للتخلص من السيليكا … أم نستخدم أنتى سكيل قوى يمنع ترسبها … أم نستخدم أغشية خاصة بالسيليكا قبل الدخول على الأغشية العادية التى تزيل الأملاح … أم نضطر إلى الغسيل الكيميائى كلما تكونت السيليكا على الأغشية علماً بأن إزالتها صعبة جداً … أم نقلل تركيز الحديد والألمونيوم كما قلنا؟ ننتظر خبراتكم الثمينة ونتمنى أن تكون من واقع خبرة عملية
بالنسبة لقشور الفوسفات فلن نخوض فيه كثيراً لأنه أقل خطورة وهو يظهر فى المعتاد مع مياه الصرف المنزلى نتيجة احتواء مساحيق الغسيل عليه خاصة البولى فوسفات.
وقشور الفوسفات مع الكالسيوم هى أشهرها وتذوب فى الوسط الحامضى … ومن المناسب جعل الpH فى المدى الحامضى عند دخول الأغشية بجانب إضافة الأنتىي سكيل
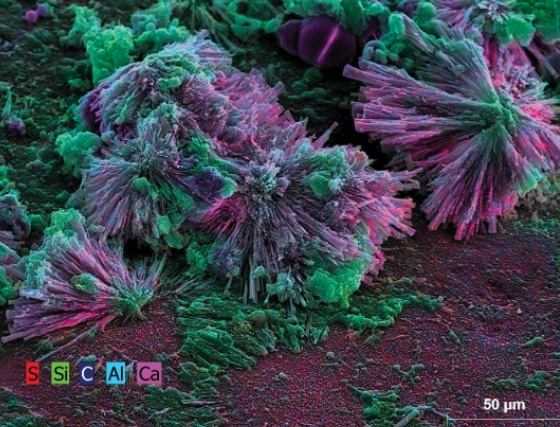
وهذه صورة مكبرة “لكوكتيل” من قشور مكونة من عدة عناصر(كبريت وسيلكون وكالسيوم وألمونيوم وكربون) تكون منظومة ملونة رائعة تشابه الشعاب المرجانية فى البحار
:
الأنتى سكيل وترسبه على الممبرين:
له عدة أنواع منه ما يترسب على الممبرين لو زادت جرعته خاصة النوع الذى يتكون من فوسفات فيترسب على هيئة Ca3PO42 ومنه ما يخرج كله مع الريجيكت ولا يترسب على الغشاء خاصة النوع المتكون من Organo phosphonate وهذا هو الأصل (ويستطيع المهندس قياسه فى الريجيكت للتأكد من هذا الكلام) … وقد ذكرنا من قبل أن الأنتى سكيل العضوى إذا تم استخدام جرعة منه أكبرمن المسموح به كون هو نفسه فاولينج على الغشاء وحدث ارتفاع فى الضغوط … وفى العموم لا يُمكن أن يمر الأنتى سكيل مع البيرميت لأن وزنه الجزيئى عالى.
أسباب تكون القشور Scaling على الأغشية:
وننوه أن الأمورالتالية ليس شرطاً أن ننفذها كلها ولكنها تعتمد على الوحدة وطبيعة مياه التغذية:
1- عدم إضافة حمض قبل دخول الماء على أغشية الRO … أو عدم إضافته بالجرعة المطلوبة (وكما قلنا أنه يخفض الرقم الهيدروجينى إلى 5.5 – 6.5 ويحول أملاح العسر من أملاح مترسبة إلى ذائبة يتم التخلص منها مع ال(Concentrate.
2- عدم إضافة مانع الترسيب الأنتيسكيلantiscale من الأساس أو عدم إضافته بالجرعة المناسبة والتى أوصت به الشركة الموردة أ وعدم استخدام antiscale مناسب … أو عدم مراعاة الرقم الهيدروجينى الذى يعمل فيه الأنتيسكيل … أحد أسباب تكون القشور.
3- حدوث تسريب للأملاح فى منطقة المعالجة الأولية كتسريب من الميسرات Softener أو من الفلاتر الرملية أو الكربونية بأى وسيلة.
4- التغير فى قيم الأملاح وتحديداً أملاح العسر فى مياه التغذية خاصة مياه الآبارالتى تمتاز أحياناً بتغير الأملاح فيها من وقت لآخر لذا يجب متابعة مياه التغذية وعمل التحاليل الدورية التى ذكرناها حتى لو حدث تغير فى التركيب يجب أن يتبعه تغير فى جرعات الحمض والأنتي سكيل.
5- الخطأ الشائع هو تشغيل المحطة بحيث يزيد الريكافارىrecovery أو الماء المنتج عن الحد المسموح به بغرض الحصول على انتاجية أعلى … والموصى به أن يكون الrecovery ما بين ال50- 80% من حجم مياه التغذية … وهذه النسبة تعتمد على الأملاح فى مياه التغذية … فكلما زادت يجب تقليل الrecovery وهذا يتم بتوصية الشركة المنتجة للأغشية بجانب خبرة العاملين بالوحدة … كما أن تحديد الريكافرى يعتمد على عمر الأغشية … وقد تحدثنا عن موضوع الريكافري بالتفصيل قبل ذلك.
6- قلنا بأننا نلجأ أحياناً فى المعالجة الإبتدائية لإضافة حمض لتقليل الpH … فبعض مصادر المياه يكون لها pH فوق ال 8.5 كمياه النيل فى بعض الفصول … مما يسبب تكون كربونات الكالسيوم شحيحة الذوبان فى الماء والتى تترسب بسهولة على الأغشية … أما بإضافة الحمض وتقليل الpH وبالتالى تقليل قيمة الLSI فيترتب عليه كيميائياً أن أملاح الكالسيوم (مثل كربونات الكالسيوم) تتحول إلى بيكربونات ذائبة مع انخفاض الpH ولا تترسب على الأغشية
والسؤال هنا … هل هناك تأثير من الحامض على مادة الغشاء؟؟
والإجابة المعتادة هو أنه يجب الرجوع إلى الشركة المصنعة وتوصياتها … وفى العموم أنه لا يوجد تأثير من الحامض على مادة الغشاء مادام فى مدى التركيزات الموصى بها … يتم ضبط معدل الحقن من خلال مضخة الحقن إما بحقن كميات قليلة من الحمض المركز أو تخفيف الحمض أولاً وزيادة معدل الحقن وذلك تبعاً لتصميم المحطة.
والحمض المعتاد الذى يتم إضافته هو حمض الهيدروكلوريك ولا يُفضل حقن الأحماض العضوية (مثل حمض الستريكCitric acid ) لأنها أحماض ضعيفة كما أنه تسبب تكون الفاولينج العضوى … إضافة إلى ذلك أن سعره مرتفع مقارنة بالأحماض الغيرعضوية …
أما أثناء عملية غسيل الغشاء فالأمر يختلف … فقد ننزل بالpH إلى 2- 2.5 فى زمن قصير… كما أننا من الممكن أن نستخدم حمض الستريك … كم سيأتى بالتفصيل فى غسيل الأغشية
وإليك تقييم لمياه التغذية بناءً على قيم الLSI والذى يتنبأ تحديداً بترسب أملاح كربونات الكالسيوم:

ملاحظات لحضراتكم:
1- قلنا أن الLSI عندما تساوى صفر فإنه لا مجال لتكون القشور وللأمانة العلمية … الكلام النظري شىء والعملي شىء آخر … قد تتكون القشور مع الزمن أو نتيجة لقياس خاطىء لمفردات الLSI أو لتغير طبيعة المياه الخام … ونلاحظ أن تكون القشور يكون عادةً فى نهايات الأغشية أو ما نسميها أغشية الذيل Tail membranes كما أوضحنا.
2- عندما نجد قيمة الLSI مرتفعة فإنه يتم خفضها بخفض قيمة الرقم الهيدروجينىpH بإضافة حمض (الهيدروكلوريك أوالكبريتيك) والقيمة المستهدفة التى تناسب التناضح العكسي هى -0.2 والتى تشير إلى نقطة ما تحت التشبع كما ذكرنا … ولو كانت القيمة أعلى من نقطة الخطر يتم إضافة أنتى سكيل.
3- بعض الشركات أحياناً تخبرنا بأن ال antiscale يعمل بفاعلية عند قيمة موجبة للLSI حتى القيمة 2.5 … لذا يمكن الإستغناء عن إضافة الحمض والإبقاء على الرقم الهيدروجينى كما هو عند LSI = +1.8 … راجع كل هذا الكلام فى الجزء الأول من الكورس.
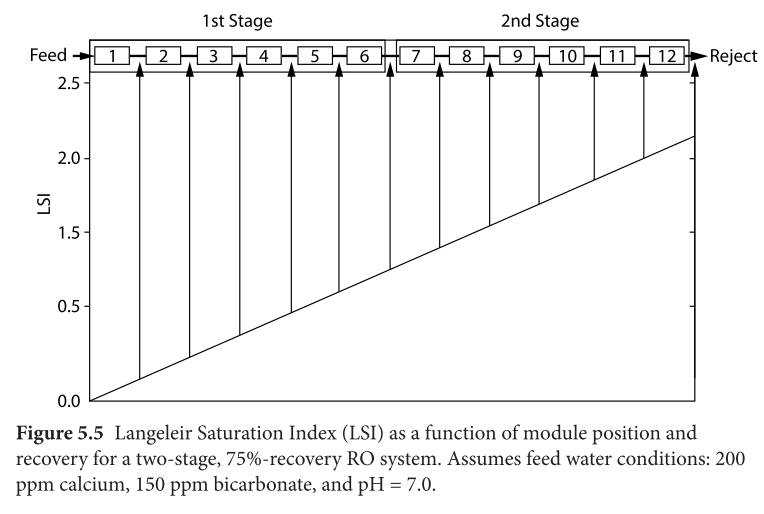
4- الرسم البيانى التالي يوضح كيف تزيد قيمة الLSI زيادة خطية مع تتابع الأغشية والمراحل … وفى أغشية الذيل تصل لقيمة فوق ال2 … يعنى امكانية ترسب القشور 100% … ولذلك يتم إضافة الأنتيسكيل فى بعض الحالات لمنع ترسب الأملاح حتى مع قيم عالية للLSI … كما يجب عدم عمل ريكافرى عالى فى أغشية الذيل وهو عامل مهم جداً بجانب الأنتى سكيل الذى ربما لا يستطيع منع ترسب القشور بالكلية حتي ولو كان أنتي سكيل قوى.
ما هى قصة الConcentration polarization؟
هى ببساطة ظاهرة تراكم الأملاح فى المياه التى تم حجزها قبل الأغشية … أملاح تمر وأنواع أخرى لا تمر بسهولة من خلال الأغشية … تتراكم هذه النوعية من الأملاح على سطح الأغشية وتكون طبقة Boundry layer أكثر تركيزاً من الأملاح فى المياه السارية فوقها … بمعنى آخر يحدث لها استقطاب على فى هذه الطبقة … وتتشكل هذه الطبقة بقوة أكبر وسُمك أكبر كلما قل الcross flow أوقلت الدوامات أو الturbulance … ويزيد بذلك الضغط الأسموزى ويقل ال net driving pressureالمسئول عن نقل المياه عبرالغشاء كما سنتحدث عنه بعد ذلك … وبالتالى يقل الflux وكمية البيرميت … كما أنه يؤثر على اختيارية الأغشية للأملاح النافذة selectivity فبالطبع الوضع يكون غير طبيعى … كما أنها بداية مهمة فى ترسب القشور … ومع الوقت يحدث تسرب فى الأملاح عبر الغشاء وانتهاء عمره ومدة خدمته … وللتغلب على هذه الظاهرة يجب تقليل الflux المار عبر الأغشية أو نزيد من كمية مياه التغذية فتزيد اضطراب المياه … بجانب عمل شبكة الfeed spacer التى تحدثنا عنها من قبل والتى تسبب اضطراب أيضاً فى المياه ونتجنب بذلك الconcentration polarization وتكون القشور.
انظر كيف تتكون ظاهرة الConcentration polarization فى الصورة التالية … حيث ترى أن تركيز الأملاح فى الboundry layer فى البداية يكون مساوٍ للطبقة السارية فوقها ويُشار إليها بالCb … ومع التقدم فى الأغشية يزيد تركيز الأملاح فى الboundry layer والتى يُشار إليها بال Cm وتكون أعلى فى تركيز الأملاح من الطبقة السارية الموازية للغشاء فوقها …
Cm > Cb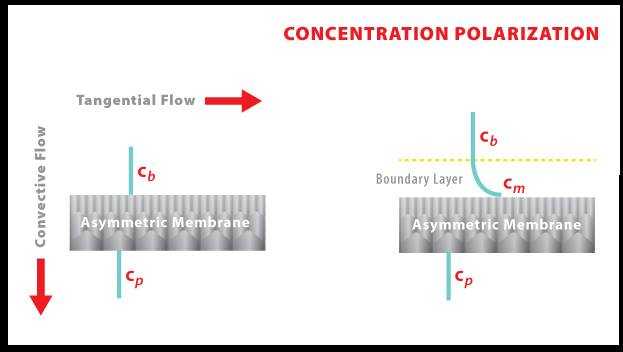
وهذه صورة أخرى لطبقة الBoundary الملاصقة للغشاء وتركز الأملاح فيها:
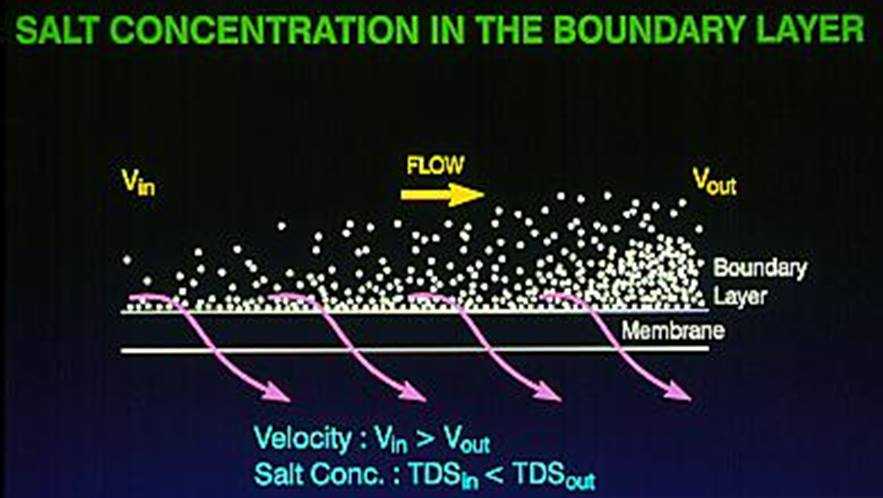
فما هو الفاكتور بيتاBeta (β) ؟؟؟
معامل بيتا هو الConcentration polarization factor وهو النسبة بين تركيز الأملاح على سطح الغشاء إلى تركيزها فى المياه السارية … ولذلك قيم البيتا العالية معناها نسب للملح عند السطح أعلى من المحلول المائى … وهو مؤشر لحدوث تراكم الفاولينج أوتكون القشور.
والقيم المقبولة لبيتا هى من 1 – 1.2 حد أقصى لتجنب تكون الفاولينج والقشور.
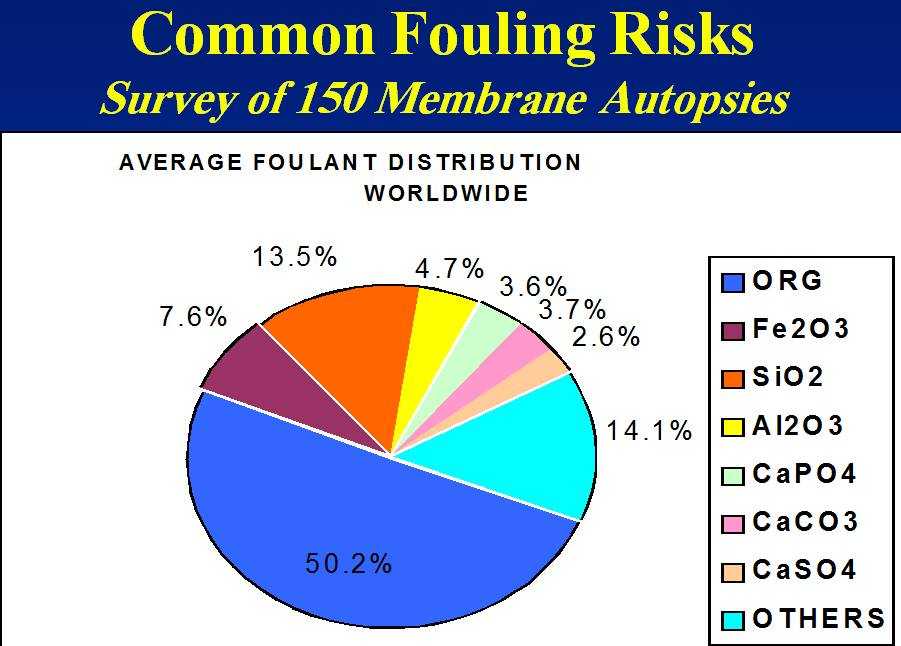
والرسم البيانى التالى هو نتيجة دراسة 150غشاء بطريقة الأوتوبساىautopsy التى سنتحدث عنها بعد ذلك … وجدنا أن الفاولينج العضوى يمثل النسبة الأكبر والأخطر من أنواع الفاولينج يليه ثانى أوكسيد السيليكون (السيليكا) ثم أكسيد الحديديك ثم أوكسيد الألمونيوم وأملاح الكالسيوم المختلفة
بخصوص تكون الرواسب بفعل تأكسد المعادن
محطة تحلية مكونه من Stage1 ومن
Stage2
بحيث أن reject المرحلة الأولى يدخل إلى المرحلة الثانية هل هناك أهمية لإضافة SMB وبالأخص قبل المرحلة الثانية للRO
الرأي مفتوح
نقول أنه يجب إضافة SMB لأنه مادة
Antioxidant
حيث يزيل أي نواتج أكسدة حيث يمنع حدوث الأكسدة للمعادن على الممبرين للمرحلة الثانية وبالتالي يمنع ترسب المعادن وعمل fouling
مؤشرات حدوث ال scal قبل تكونه على الأغشية
السكيل scale تتكون نتيجة وجود عناصر قابلة للترسيب عند وصولها لتراكيز معينة ودور حضرتك أن لا توصل لدرجة التركيز التي يبدأ عندها بالترسب عن طريق
1-تحديد نسبة ال recovery الصحيحة
2-ضبط مانع الترسيب
3- المتابعة المستمرة والدورية في بداية التشغيل ومتابعة الأغشية الأخيرة من ناحية الصرف عن طريق وزنها
4- النظر إلى بداية تكون البلورات وذلك بالملمس الخشن الخاص بالغشاء فإذا كان الملمس خشن أقرب لورق الصنفرة يعطي مؤشر لبداية تكون رواسب
والرواسب نوعان
1-يذوب في الأحماض مثل الكربونات ترسبات أقرب للجيرية الغير إبرية
2-يذوب في القواعد مثل السالفيت بلورات إبرية شديدة اللمعان
هناك ملحوظه ..
تذداد السيلكا عند التكاثر الموسمي للدياتوم (Diatom ) وهو طحلب من خليه واحده جدرانه مشبعه بالسيلكا وكذالك هياكله….
وتلحظ ذياده في السيلكا في مياه النيل في اوقات معينه ويعود الوضع طبيعيا بعد ذالك…
انا عندي ترتفع السيلكا في فرع دمياط في شهري 9-10
السيلكا بتذيد الي 10.0ppm
وباقي شهور السنه حولين ال 2.0ppm
2.0ppm
السلام عليكم ورحمة الله وبركاته
بارك الله فيكم
ما تقدمونه من معلومات للمختصين والعاملين في هذا المجال عمل مقدس يجعل من مؤسستكم العامرة مؤسسة رسالة
هذا المنهج لا يدرس في الجامعات إلا القليل منها وفي بعض الدول المتقدمة وينتشر الان في كثير من البلدان كما نحن في السودان والكل يعمل والحوجة تجعل المنتج مرغوب فيه ولكن لا يخطر على بالنا أن هذه التقنية تحتاج لمعرفة علمية دقيقة ومعقدة ولابد من متابعتها خوفا على تعقيدات ممكن تصيب الإنسان والذي استبدل ماء غير متوفر وان وجد فهو غير شفاف بماء نقي شفاف ولربما يحمل ما لا تحمد عقباه خاصة التلوث الكيميائي……
بارك الله فيكم